邁威生物 (688062.SH),一家全產業鏈布局的創新型生物制藥公司,宣布其自主研發的 9MW3811 注射液于近日正式獲得澳大利亞治療用品管理局 (TGA) 批準開展臨床試驗。9MW3811 注射液適應癥為多種晚期惡性腫瘤以及纖維化疾病。目前,9MW3811 是全球同靶點藥物中首個開展臨床試驗的單抗品種。
9MW3811 是創新靶點人源化單克隆抗體,可高效阻斷 IL-11 下游信號通路的激活,從而達到對纖維化和腫瘤的治療效果。
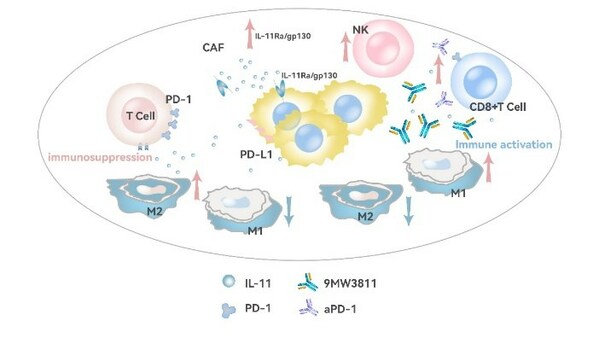
9MW3811 的抗腫瘤作用機制
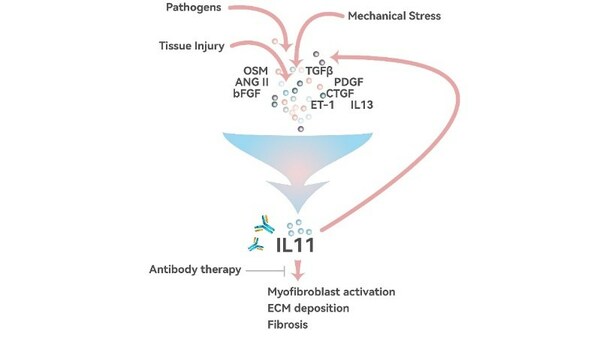
9MW3811 的抗纖維化作用機制
9MW3811 是第一款進入臨床階段的靶向 IL-11 的單克隆抗體,也是 IL-11 靶點第一款進入臨床階段的非重組蛋白藥物。
關于邁威生物
邁威生物(688062.SH) 是一家全產業鏈布局的創新型生物制藥公司,始終秉承"讓創新從夢想變成現實"的愿景,踐行"探索生命,惠及健康"的使命,通過源頭創新,為患者提供療效更好、可及性更強的生物創新藥,滿足全球未被滿足的臨床需求。2017 年成立以來,邁威生物構建了以抗體藥物靶點發現與分子發現為起點,覆蓋成藥性研究、臨床前研究、臨床研究和生產轉化等藥品研發全周期的創新體系,實現集研發、生產、營銷于一體的全產業鏈布局。我們專注于腫瘤和年齡相關疾病,涉及自身免疫、腫瘤、代謝、眼科、感染等治療領域,憑借國際領先的五項特色技術平臺和研發創新能力,建立了豐富且具有競爭力的管線。現有 16 個品種處于不同階段,包括 12 個創新品種和 4 個生物類似藥,其中 1 個品種上市,2 個品種上市申請獲得受理,3 個品種處于關鍵注冊臨床試驗階段。并獨立承擔 1 項國家"重大新藥創制"重大科技專項、2 項國家重點研發計劃和多個省市級科技創新項目。邁威生物以創新為本,注重產業轉化,符合中國 NMPA、美國 FDA、歐盟 EMA GMP標準的抗體和重組蛋白藥物產業化基地已在江蘇泰州投入使用,并已通過歐盟 QP 審計,位于上海金山和江蘇泰州的大規模商業化生產基地正在建設中。
(新媒體責編:wa12)
聲明:
1、凡本網注明“人民交通雜志”/人民交通網,所有自采新聞(含圖片),如需授權轉載應在授權范圍內使用,并注明來源。
2、部分內容轉自其他媒體,轉載目的在于傳遞更多信息,并不代表本網贊同其觀點和對其真實性負責。
3、如因作品內容、版權和其他問題需要同本網聯系的,請在30日內進行。電話:010-67683008
人民交通24小時值班手機:17801261553 商務合作:010-67683008轉602 E-mail:[email protected]
Copyright 人民交通雜志 All Rights Reserved 版權所有 復制必究 百度統計 地址:北京市豐臺區南三環東路6號A座四層
增值電信業務經營許可證號:京B2-20201704 本刊法律顧問:北京京師(蘭州)律師事務所 李大偉
 京公網安備 11010602130064號 京ICP備18014261號-2 廣播電視節目制作經營許可證:(京)字第16597號
京公網安備 11010602130064號 京ICP備18014261號-2 廣播電視節目制作經營許可證:(京)字第16597號



